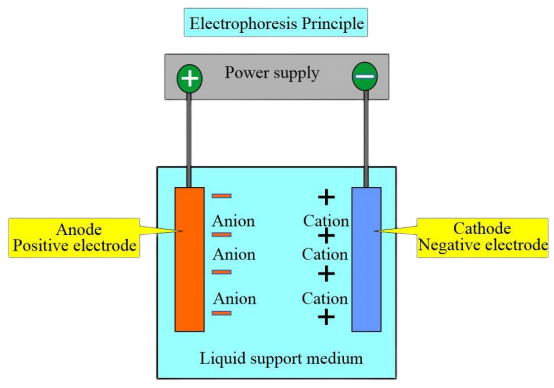
Принцип на експеримента
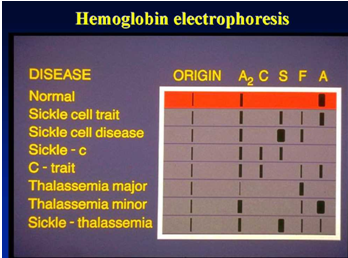
Електрофорезата на хемоглобина има за цел да открие и потвърди различни нормални и абнормни хемоглобини.
Поради различните заряди и изоелектрични точки на различните типове хемоглобин, в буферен разтвор с определено pH, когато изоелектричната точка на хемоглобина е по-ниска от pH на буферния разтвор, хемоглобинът носи отрицателен заряд и мигрира към анода по време на електрофореза. Обратно, хемоглобинът с положителен заряд се движи към катода.
При определено напрежение и след определено време за електрофореза хемоглобините с различни заряди и молекулни тегла показват различни посоки и скорости на миграция. Това позволява разделянето на отделни зони и последващ колориметричен или електрофоретичен сканиращ анализ може да се извърши върху тези зони за количествено определяне на различни хемоглобини. Най-често използваният метод е мембранна електрофореза с целулозен ацетат pH 8,6.
В рамките на цитоплазмата етиленгликоловите групи (CHOH-CHOH), присъстващи в гликоген или полизахаридни вещества (като мукополизахариди, мукопротеини, гликопротеини, гликолипиди и др.), се окисляват от периодна киселина и се превръщат в алдехидни групи (CHO-CHO). Тези алдехидни групи се комбинират с безцветния лилаво-червен реактив на Шиф, образувайки лилаво-червено багрило, което се отлага там, където в клетката има полизахариди. Тази реакция е известна като оцветяване с периодична киселина-Шиф (PAS), по-рано наричано оцветяване с гликоген.
Метод на експеримента
Материали:Целулозен ацетатмембрана, апарат за електрофореза(DYCP-38C и захранване DYY-6C), Превъзходен инструмент за зареждане на проби (пипета), спектрофотометър, колориметрични кювети, буфери.
Буфер:
(1) pH 8,6 TEB буфер: Претеглете 10,29 g Tris, 0,6 g EDTA, 3,2 g борна киселина и добавете дестилирана вода към 1000 ml.
(2) Боратен буфер: Претеглете 6,87 g боракс и 5,56 g борна киселина и добавете дестилирана вода към 1000 ml.
Процедура:
Pвъзстановяване на разтвор на хемоглобин
Вземете 3 ml кръв, съдържаща хепарин или натриев цитрат като антикоагулант. Центрофугирайте при 2000 rpm за 10 минути и изхвърлете плазмата. Промийте червените кръвни клетки три пъти с физиологичен разтвор (750 rpm, 5 минути центрофугиране всеки път). Центрофугирайте при 2200 rpm за 10 минути и изхвърлете супернатантата. Добавете равно количество дестилирана вода, след което добавете 0,5 пъти обема тетрахлорметан. Разклатете енергично в продължение на 5 минути и след това центрофугирайте при 2200 rpm в продължение на 10 минути, за да съберете горния Hb разтвор за по-късна употреба.
Накисване на мембраната
Нарежете мембраната от целулозен ацетат на ивици с размери 3 cm × 8 cm. Накиснете ги в буфер с pH 8,6 TEB до пълно насищане, след това извадете и изсушете с филтърна хартия.
Зацапване
Използвайте пипета, за да нанесете 10 μl от разтвора на хемоглобина вертикално върху мембраната от целулозен ацетат (грапавата страна), на около 1,5 cm от ръба.
Електрофореза
Изсипете боратния буферен разтвор в камерата за електрофореза. Поставете мембраната от целулозен ацетат с петниста страна в края на катода на камерата. Работете на 200 V за 30 минути.
Елуиране
Изрежете зоните HbA и HbA2, поставете ги в отделни епруветки и добавете съответно 15 ml и 3 ml дестилирана вода. Внимателно разклатете, за да елуирате напълно хемоглобина, след това разбъркайте.
Колориметрия
Нулирайте абсорбцията, като използвате дестилирана вода за елуиращия разтвор и измерете абсорбцията при 415 nm.
Изчисляване
HbA2(%) = Абсорбция на епруветка HbA2 / (Абсорбция на епруветка HbA × 5 + абсорбция на епруветка HbA2) × 100%
Изчисляване на експериментални резултати
Референтен обхват за pH 8,6 TEB буферна електрофореза с целулозен ацетат: HbA > 95%, HbA2 1%-3,1%
Бележки
Времето за електрофореза не трябва да бъде твърде дълго. Мембраната от целулозен ацетат не трябва да изсъхва по време на електрофореза. Спрете електрофорезата, когато HbA и HbA2 са ясно разделени. Продължителната електрофореза може да причини дифузия на лентата и замъгляване.
Избягвайте да използвате твърде много проба. Прекомерното количество течен хемоглобин може да доведе до отлепване на лентата или недостатъчно оцветяване, което води до фалшиво повишени нива на HbA.
Предотвратете замърсяването на мембраната от целулозен ацетат с протеини.
Токът не трябва да е твърде висок; в противен случай хемоглобиновите ленти може да не се разделят.
Винаги включвайте проби от нормални индивиди и необходими известни анормални хемоглобини като контроли.
Beijing Liuyi Biotechnology произвежда професионалния резервоар за електрофореза за електрофореза на хемоглобин, който е моделътDYCP-38Cрезервоар за електрофореза с мембрана от целулозен ацетат и има два модела захранване за електрофореза, налични за резервоара за електрофореза с мембрана от целулозен ацетатDYY-2CиDYY-6Cзахранване.
Междувременно Beijing Liuyi Biotechnology предоставя мембрана от целулозен ацетат за клиентите и размерът на мембраната от целулозен ацетат може да бъде персонализиран. Добре дошли да ни попитате за мостри и повече информация.
Марката Beijing Liuyi има повече от 50-годишна история в Китай и компанията може да осигури стабилни и висококачествени продукти по целия свят. След години на развитие, той е достоен за вашия избор!
Сега търсим партньори, както OEM резервоар за електрофореза, така и дистрибутори са добре дошли.
Ако имате някакъв план за закупуване на нашите продукти, моля, не се колебайте да се свържете с нас. Можете да ни изпратите съобщение на имейл[имейл защитен]или[имейл защитен], или моля, обадете ни се на +86 15810650221 или добавете Whatsapp +86 15810650221, или Wechat: 15810650221
Време на публикуване: 20 септември 2023 г